Struktur Lewis adalah konsep penting dalam ilmu kimia yang digunakan untuk menggambarkan distribusi elektron valensi dalam suatu molekul. Dengan memahami struktur Lewis, kita dapat memahami bagaimana atom-atom saling berikatan, terutama dalam ikatan kovalen. Konsep ini sangat berguna dalam menentukan bentuk molekul, sifat kepolaran, dan jenis ikatan yang terbentuk antara atom-atom. Struktur Lewis juga membantu kita memahami bagaimana atom mencapai kestabilan melalui pemakaian pasangan elektron bersama.
Dalam artikel ini, kita akan membahas secara lengkap pengertian struktur Lewis, cara menggambarnya, serta contoh-contoh struktur Lewis dari berbagai senyawa. Kami juga akan menjelaskan langkah-langkah praktis untuk menggambar struktur Lewis, sehingga Anda dapat memahami dan menerapkannya dengan mudah.
Struktur Lewis diperkenalkan oleh Gilbert N. Lewis pada tahun 1916 dalam artikelnya yang berjudul "The Atom and the Molecule". Tujuan dari struktur ini adalah untuk menunjukkan bagaimana elektron-elektron valensi dari setiap atom berperan dalam pembentukan ikatan kimia. Elektron valensi yang digambarkan dalam struktur Lewis biasanya dilambangkan dengan tanda titik (.) atau silang (x), dan pasangan elektron yang digunakan bersama bisa ditunjukkan dengan garis.
Dalam ikatan kovalen, atom-atom nonlogam saling berbagi elektron agar mencapai kestabilan, yaitu memiliki konfigurasi elektron seperti gas mulia. Kestabilan ini bisa berupa kestabilan duplet (2 elektron) atau oktet (8 elektron). Dengan memahami struktur Lewis, kita dapat mengetahui bagaimana atom-atom tersebut berikatan dan bagaimana mereka mencapai kestabilan.
Selain itu, struktur Lewis juga memberikan informasi tentang jumlah pasangan elektron bebas (PEB) dan pasangan elektron ikatan (PEI) dalam suatu molekul. Hal ini sangat penting dalam menentukan bentuk molekul dan sifat-sifat kimianya. Misalnya, molekul dengan banyak PEB cenderung memiliki bentuk yang lebih kompleks dibandingkan molekul dengan sedikit PEB.
Keseluruhan penjelasan ini akan membantu Anda memahami konsep struktur Lewis secara mendalam dan mampu menggambar struktur Lewis dari berbagai senyawa. Mari kita lanjutkan dengan penjelasan detail mengenai pengertian struktur Lewis dan cara menggambarnya.
Pengertian Struktur Lewis
Struktur Lewis adalah model visual yang digunakan untuk menggambarkan distribusi elektron valensi dalam suatu molekul. Elektron valensi adalah elektron yang berada di kulit terluar suatu atom dan berperan dalam pembentukan ikatan kimia. Dalam struktur Lewis, elektron valensi ini dilambangkan dengan tanda titik (.) atau tanda silang (x), sedangkan pasangan elektron yang digunakan bersama ditunjukkan dengan garis.
Konsep ini diperkenalkan oleh Gilbert N. Lewis pada tahun 1916 dalam artikelnya yang berjudul "The Atom and the Molecule". Tujuan utama dari struktur Lewis adalah untuk menunjukkan bagaimana atom-atom saling berikatan melalui pemakaian pasangan elektron bersama, terutama dalam ikatan kovalen. Dengan memahami struktur Lewis, kita dapat mengetahui bagaimana atom-atom mencapai kestabilan dan apa jenis ikatan yang terbentuk antara mereka.
Struktur Lewis juga sering disebut sebagai diagram titik Lewis atau rumus titik elektron. Dalam struktur ini, setiap atom digambarkan dengan simbolnya dan dikelilingi oleh tanda titik atau silang yang mewakili elektron valensinya. Pasangan elektron yang digunakan bersama ditunjukkan dengan garis, dan pasangan elektron bebas (PEB) yang tidak digunakan dalam ikatan juga digambarkan.
Pemahaman tentang struktur Lewis sangat penting dalam memahami sifat-sifat kimia suatu molekul, seperti kepolaran, bentuk molekul, dan reaktivitas. Selain itu, struktur Lewis juga membantu dalam menentukan jenis ikatan yang terbentuk antara atom-atom, baik itu ikatan tunggal, rangkap dua, maupun rangkap tiga.
Dalam struktur Lewis, atom pusat umumnya merupakan atom yang jumlahnya paling sedikit dalam molekul. Contohnya, dalam molekul NH3, atom nitrogen (N) menjadi atom pusat karena jumlahnya hanya satu, sedangkan atom hidrogen (H) jumlahnya tiga. Setelah menentukan atom pusat, kita kemudian memasangkan elektron dari atom-atom tersebut hingga semua atom mencapai kestabilan, baik itu kestabilan duplet (untuk atom hidrogen) maupun kestabilan oktet (untuk sebagian besar atom lainnya).
Dengan demikian, struktur Lewis bukan hanya sekadar gambar visual, tetapi juga alat penting dalam memahami interaksi antar atom dan sifat-sifat kimia molekul-molekul yang terbentuk.
Cara Menggambar Struktur Lewis
Menggambar struktur Lewis adalah proses yang cukup sederhana jika kita mengikuti langkah-langkah yang tepat. Berikut adalah panduan lengkap untuk menggambar struktur Lewis:
Langkah 1: Tentukan Jumlah Elektron Valensi
Langkah pertama dalam menggambar struktur Lewis adalah menentukan jumlah elektron valensi dari setiap atom dalam molekul. Elektron valensi adalah elektron yang berada di kulit terluar atom dan berperan dalam pembentukan ikatan. Untuk mengetahui jumlah elektron valensi, kita bisa melihat konfigurasi elektron dari atom tersebut.
Contoh: - Atom karbon (C) memiliki konfigurasi elektron 2, 4, sehingga memiliki 4 elektron valensi. - Atom hidrogen (H) memiliki konfigurasi elektron 1, sehingga memiliki 1 elektron valensi.
Langkah 2: Tentukan Atom Pusat
Atom pusat adalah atom yang jumlahnya paling sedikit dalam molekul. Biasanya, atom pusat adalah atom yang memiliki kecenderungan lebih tinggi untuk berikatan dengan atom-atom lainnya.
Contoh: - Dalam molekul NH3, atom nitrogen (N) menjadi atom pusat karena jumlahnya hanya satu, sedangkan atom hidrogen (H) jumlahnya tiga. - Dalam molekul CH4, atom karbon (C) menjadi atom pusat karena jumlahnya hanya satu, sedangkan atom hidrogen (H) jumlahnya empat.
Langkah 3: Gambarkan Atom Pusat dan Atom Lain
Setelah menentukan atom pusat, kita perlu menggambarkan atom pusat di tengah-tengah dan atom-atom lainnya mengelilinginya. Misalnya, dalam molekul NH3, kita akan menggambarkan atom nitrogen di tengah dan tiga atom hidrogen mengelilinginya.
Langkah 4: Pasangkan Elektron
Langkah selanjutnya adalah memasangkan elektron dari atom-atom tersebut hingga semua atom mencapai kestabilan. Kestabilan ini bisa berupa kestabilan duplet (2 elektron) atau kestabilan oktet (8 elektron).
Contoh: - Dalam molekul CH4, atom karbon membutuhkan 4 elektron tambahan untuk mencapai kestabilan oktet. Oleh karena itu, kita akan memasangkan 1 elektron dari atom karbon dengan 1 elektron dari setiap atom hidrogen, sehingga terbentuk 4 pasang elektron ikatan (PEI). - Dalam molekul NH3, atom nitrogen membutuhkan 3 elektron tambahan untuk mencapai kestabilan oktet. Oleh karena itu, kita akan memasangkan 1 elektron dari atom nitrogen dengan 1 elektron dari setiap atom hidrogen, sehingga terbentuk 3 pasang elektron ikatan (PEI).
Langkah 5: Periksa Kembali Gambar
Setelah memasangkan elektron, kita perlu memeriksa apakah semua atom sudah mencapai kestabilan. Jika semua atom sudah memiliki 8 elektron (untuk kestabilan oktet) atau 2 elektron (untuk kestabilan duplet), maka struktur Lewis sudah benar.
Contoh: - Dalam molekul CH4, atom karbon memiliki 8 elektron dan setiap atom hidrogen memiliki 2 elektron, sehingga struktur Lewis sudah benar. - Dalam molekul NH3, atom nitrogen memiliki 8 elektron dan setiap atom hidrogen memiliki 2 elektron, sehingga struktur Lewis sudah benar.
Dengan mengikuti langkah-langkah di atas, kita dapat menggambar struktur Lewis dari berbagai senyawa dengan mudah dan akurat.
Contoh Struktur Lewis
Berikut adalah beberapa contoh struktur Lewis dari berbagai senyawa yang dapat membantu Anda memahami cara menggambarkannya:
1. Struktur Lewis Molekul NH3 (Amonia)
- Atom Pusat: Nitrogen (N)
- Elektron Valensi:
- Nitrogen (N): 5 elektron valensi
- Hidrogen (H): 1 elektron valensi per atom
- Langkah Menggambar:
- Letakkan atom nitrogen di tengah dan tiga atom hidrogen mengelilinginya.
- Pasangkan 1 elektron dari nitrogen dengan 1 elektron dari setiap atom hidrogen, membentuk 3 pasang elektron ikatan (PEI).
- Periksa apakah nitrogen telah memiliki 8 elektron (kestabilan oktet) dan setiap hidrogen memiliki 2 elektron (kestabilan duplet).
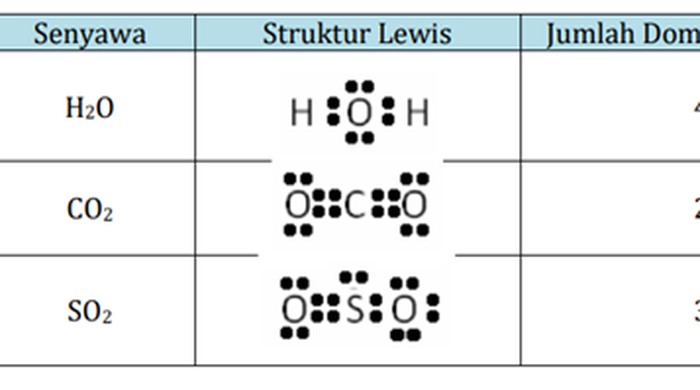
2. Struktur Lewis Molekul H2O (Air)
- Atom Pusat: Oksigen (O)
- Elektron Valensi:
- Oksigen (O): 6 elektron valensi
- Hidrogen (H): 1 elektron valensi per atom
- Langkah Menggambar:
- Letakkan atom oksigen di tengah dan dua atom hidrogen mengelilinginya.
- Pasangkan 1 elektron dari oksigen dengan 1 elektron dari setiap atom hidrogen, membentuk 2 pasang elektron ikatan (PEI).
- Sisa 2 elektron oksigen akan menjadi pasangan elektron bebas (PEB).
- Periksa apakah oksigen memiliki 8 elektron (kestabilan oktet) dan setiap hidrogen memiliki 2 elektron (kestabilan duplet).
3. Struktur Lewis Molekul CO2 (Karbon Dioksida)
- Atom Pusat: Karbon (C)
- Elektron Valensi:
- Karbon (C): 4 elektron valensi
- Oksigen (O): 6 elektron valensi per atom
- Langkah Menggambar:
- Letakkan atom karbon di tengah dan dua atom oksigen mengelilinginya.
- Pasangkan 2 elektron dari karbon dengan 2 elektron dari setiap atom oksigen, membentuk 2 pasang elektron ikatan (PEI) yang merupakan ikatan rangkap dua.
- Periksa apakah karbon memiliki 8 elektron (kestabilan oktet) dan setiap oksigen memiliki 8 elektron (kestabilan oktet).
4. Struktur Lewis Molekul CH4 (Metana)
- Atom Pusat: Karbon (C)
- Elektron Valensi:
- Karbon (C): 4 elektron valensi
- Hidrogen (H): 1 elektron valensi per atom
- Langkah Menggambar:
- Letakkan atom karbon di tengah dan empat atom hidrogen mengelilinginya.
- Pasangkan 1 elektron dari karbon dengan 1 elektron dari setiap atom hidrogen, membentuk 4 pasang elektron ikatan (PEI).
- Periksa apakah karbon memiliki 8 elektron (kestabilan oktet) dan setiap hidrogen memiliki 2 elektron (kestabilan duplet).
Dengan memahami contoh-contoh di atas, Anda akan lebih mudah menggambar struktur Lewis dari berbagai senyawa. Praktik reguler akan meningkatkan pemahaman dan keterampilan Anda dalam menggambar struktur Lewis.
Fungsi dan Kelebihan Struktur Lewis
Struktur Lewis memiliki berbagai fungsi dan kelebihan yang membuatnya menjadi alat penting dalam studi kimia. Salah satu fungsi utamanya adalah untuk menggambarkan distribusi elektron valensi dalam suatu molekul, sehingga kita dapat memahami bagaimana atom-atom saling berikatan dan mencapai kestabilan. Selain itu, struktur Lewis juga membantu dalam menentukan jenis ikatan yang terbentuk antara atom-atom, baik itu ikatan tunggal, ikatan rangkap dua, maupun ikatan rangkap tiga.
Kelebihan lain dari struktur Lewis adalah kemampuannya dalam menunjukkan jumlah pasangan elektron bebas (PEB) dan pasangan elektron ikatan (PEI) dalam suatu molekul. Informasi ini sangat penting dalam menentukan bentuk molekul dan sifat-sifat kimianya. Misalnya, molekul dengan banyak PEB cenderung memiliki bentuk yang lebih kompleks dibandingkan molekul dengan sedikit PEB.
Selain itu, struktur Lewis juga membantu dalam memahami sifat kepolaran suatu molekul. Molekul yang memiliki perbedaan keelektronegatifan antara atom-atomnya cenderung bersifat polar, sedangkan molekul yang memiliki keelektronegatifan yang sama cenderung bersifat nonpolar. Dengan menggunakan struktur Lewis, kita dapat menentukan apakah suatu molekul bersifat polar atau nonpolar.
Struktur Lewis juga digunakan dalam prediksi reaktivitas molekul. Molekul yang memiliki pasangan elektron bebas cenderung lebih reaktif karena pasangan elektron bebas dapat bertindak sebagai donor elektron dalam reaksi kimia. Dengan memahami struktur Lewis, kita dapat memprediksi bagaimana suatu molekul akan bereaksi dengan molekul lain.
Selain itu, struktur Lewis memberikan wawasan tentang cara atom-atom berikatan dalam senyawa. Dengan menggambarkan struktur Lewis, kita dapat memahami bagaimana atom-atom saling berikatan melalui pemakaian pasangan elektron bersama, terutama dalam ikatan kovalen.
Dengan semua fungsi dan kelebihan ini, struktur Lewis menjadi alat penting dalam memahami struktur dan sifat-sifat molekul. Dengan mempelajari struktur Lewis, kita dapat memahami lebih dalam tentang dunia kimia dan bagaimana molekul-molekul berinteraksi satu sama lain.


0Komentar