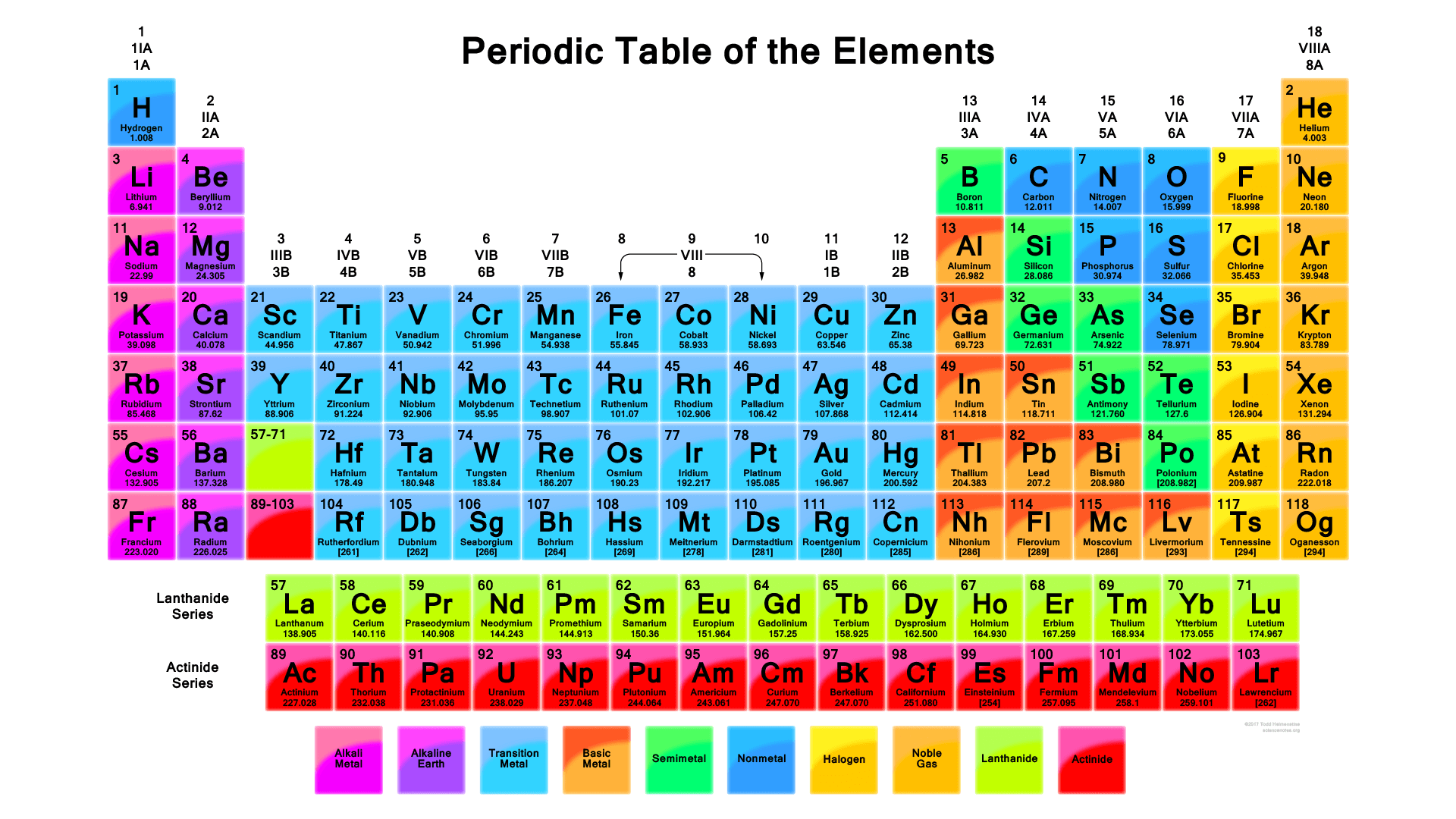
Pengertian dan Struktur Sistem Periodik Unsur Kimia yang Wajib Dipahami
Sistem Periodik Unsur (SPU) adalah salah satu fondasi penting dalam memahami sifat-sifat kimia dari berbagai unsur. Dengan struktur yang teratur dan logis, tabel periodik memberikan informasi tentang sifat fisika dan kimia setiap elemen, serta hubungan antara satu sama lainnya. Dalam dunia pendidikan, SPU menjadi salah satu materi yang wajib dipelajari oleh siswa dan mahasiswa di bidang ilmu kimia. Tidak hanya sebagai alat bantu dalam belajar, sistem ini juga menjadi dasar untuk memprediksi sifat-sifat unsur yang belum ditemukan atau belum diketahui.
Struktur SPU dibentuk berdasarkan nomor atom dan kemiripan sifat kimia. Setiap unsur ditempatkan dalam kotak tertentu dengan informasi seperti lambang unsur, nomor atom, dan massa atom. Susunan ini membentuk barisan horizontal (periode) dan barisan vertikal (golongan). Periode menunjukkan jumlah kulit elektron, sedangkan golongan menunjukkan jumlah elektron valensi. Hal ini sangat penting dalam memahami bagaimana unsur-unsur bereaksi dan membentuk senyawa.
Selain itu, SPU juga mencerminkan sifat-sifat periodik seperti jari-jari atom, energi ionisasi, afinitas elektron, dan elektronegativitas. Sifat-sifat ini mengikuti pola tertentu sepanjang periode dan golongan, yang membantu para ilmuwan dan pelajar memahami perubahan sifat kimia dari satu unsur ke unsur lainnya. Dengan demikian, SPU tidak hanya berguna dalam pembelajaran kimia, tetapi juga dalam pengembangan teknologi dan penemuan baru di bidang kimia dan material.
Pengertian Sistem Periodik Unsur
Sistem Periodik Unsur (SPU) adalah penyusunan unsur-unsur kimia berdasarkan urutan nomor atom dan sifat-sifat kimia yang mirip. Istilah "periodik" merujuk pada pola pengulangan sifat-sifat unsur yang muncul secara berkala seiring dengan meningkatnya nomor atom. Sistem ini pertama kali dikembangkan oleh Dmitri Mendeleev pada tahun 1869, yang merupakan langkah besar dalam memahami struktur dan sifat kimia dari unsur-unsur.
Dalam SPU modern, setiap unsur ditempatkan dalam kotak yang berisi informasi dasar seperti lambang unsur, nomor atom, dan massa atom. Kotak-kotak ini disusun dalam barisan horizontal (periode) dan barisan vertikal (golongan). Periode menggambarkan jumlah kulit elektron, sedangkan golongan menunjukkan jumlah elektron valensi. Hal ini membuat SPU menjadi alat yang sangat berguna untuk memprediksi sifat-sifat kimia dari suatu unsur berdasarkan posisinya dalam tabel.
Seiring perkembangan ilmu pengetahuan, SPU terus diperbaiki dan disempurnakan. Pada sistem IUPAC (International Union of Pure and Applied Chemistry) yang digunakan saat ini, golongan diberi nomor dari 1 hingga 18 tanpa menggunakan huruf A atau B. Sistem ini lebih akurat dalam menjelaskan hubungan antara sifat-sifat kimia dan struktur atom. Dengan demikian, SPU tidak hanya menjadi alat bantu dalam pembelajaran, tetapi juga menjadi dasar bagi penelitian dan pengembangan di bidang kimia.
Struktur Sistem Periodik Unsur
Struktur Sistem Periodik Unsur (SPU) terdiri dari beberapa komponen utama, yaitu periode, golongan, dan konfigurasi elektron. Setiap unsur ditempatkan dalam kotak tertentu yang mengandung informasi dasar seperti lambang unsur, nomor atom, dan massa atom. Kotak-kotak ini disusun dalam barisan horizontal (periode) dan barisan vertikal (golongan), sehingga membentuk susunan yang logis dan mudah dipahami.
Periode dalam SPU menggambarkan jumlah kulit elektron yang dimiliki oleh suatu unsur. Ada tujuh periode dalam SPU modern, mulai dari periode 1 hingga periode 7. Semakin tinggi nomor periode, semakin banyak jumlah kulit elektron yang dimiliki oleh unsur tersebut. Misalnya, unsur dalam periode 1 memiliki satu kulit elektron, sedangkan unsur dalam periode 2 memiliki dua kulit elektron, dan seterusnya.
Golongan dalam SPU menunjukkan jumlah elektron valensi yang dimiliki oleh suatu unsur. Golongan diberi nomor dari 1 hingga 18 dalam sistem IUPAC modern. Unsur-unsur dalam satu golongan memiliki sifat-sifat kimia yang mirip karena memiliki konfigurasi elektron yang serupa. Misalnya, unsur-unsur dalam golongan 1A (golongan alkali) memiliki satu elektron valensi dan cenderung bereaksi kuat dengan air, sedangkan unsur-unsur dalam golongan 7A (golongan halogen) memiliki tujuh elektron valensi dan cenderung bereaksi kuat dengan logam.
Konfigurasi elektron juga memainkan peran penting dalam struktur SPU. Elektron dalam atom terdistribusi dalam kulit-kulit elektron, dan setiap kulit memiliki jumlah maksimum elektron yang dapat ditampung. Konfigurasi ini menentukan sifat kimia dari suatu unsur, termasuk kemampuannya untuk bereaksi dan membentuk ikatan kimia.
Sifat-Sifat Periodik dalam Sistem Periodik Unsur
Dalam Sistem Periodik Unsur (SPU), sifat-sifat kimia dan fisika dari unsur-unsur mengikuti pola yang dapat diprediksi. Beberapa sifat periodik yang paling penting meliputi jari-jari atom, energi ionisasi, afinitas elektron, dan elektronegativitas. Memahami sifat-sifat ini sangat penting dalam memprediksi reaktivitas dan sifat kimia dari suatu unsur.
Jari-Jari Atom
Jari-jari atom adalah ukuran jarak antara inti atom dan elektron terluarnya. Dalam satu golongan, jari-jari atom cenderung bertambah dari atas ke bawah karena penambahan kulit elektron. Sebaliknya, dalam satu periode, jari-jari atom cenderung berkurang dari kiri ke kanan karena peningkatan muatan inti efektif yang menarik elektron lebih kuat ke arah inti.
Energi Ionisasi
Energi ionisasi adalah energi yang diperlukan untuk melepaskan satu elektron dari atom netral dalam fase gas. Dalam satu golongan, energi ionisasi cenderung menurun dari atas ke bawah karena jarak elektron terluar dari inti meningkat. Dalam satu periode, energi ionisasi cenderung meningkat dari kiri ke kanan karena peningkatan muatan inti efektif.
Afinitas Elektron
Afinitas elektron adalah ukuran kemampuan atom untuk menerima elektron. Dalam satu golongan, afinitas elektron biasanya menurun dari atas ke bawah, meskipun ada pengecualian. Dalam satu periode, afinitas elektron cenderung meningkat dari kiri ke kanan, terutama sampai golongan 7A.
Elektronegativitas
Elektronegativitas adalah ukuran kemampuan atom untuk menarik pasangan elektron dalam ikatan kimia. Dalam satu golongan, elektronegativitas cenderung menurun dari atas ke bawah karena peningkatan jarak antara inti dan elektron. Dalam satu periode, elektronegativitas cenderung meningkat dari kiri ke kanan karena peningkatan muatan inti efektif.
Klasifikasi Unsur dalam Sistem Periodik Unsur
Dalam Sistem Periodik Unsur (SPU), unsur-unsur diklasifikasikan berdasarkan sifat-sifat kimia dan fisika mereka. Terdapat tiga kelompok utama, yaitu logam, non-logam, dan metaloid. Setiap kelompok memiliki karakteristik unik yang memengaruhi sifat kimia dan reaktivitasnya.
Logam
Unsur-unsur logam umumnya memiliki sifat konduktivitas listrik dan panas yang baik, serta dapat ditempa dan ditarik menjadi kawat (ductile). Contoh logam meliputi besi, tembaga, dan aluminium. Logam biasanya berada di sebelah kiri dan tengah SPU, terutama dalam golongan 1A, 2A, dan logam transisi.
Non-logam
Unsur-unsur non-logam umumnya tidak konduktif, rapuh, dan tidak dapat ditempa. Mereka cenderung berwujud gas atau padat pada suhu ruang. Contoh non-logam meliputi oksigen, karbon, dan klorin. Non-logam biasanya berada di sebelah kanan SPU, terutama dalam golongan 6A, 7A, dan 8A.
Metaloid
Metaloid memiliki sifat yang berada di antara logam dan non-logam. Mereka bisa bersifat konduktif dalam kondisi tertentu, tetapi tidak sepenuhnya seperti logam. Contoh metaloid meliputi silikon, boron, dan arsenik. Metaloid biasanya berada di sepanjang garis batas antara logam dan non-logam di SPU.
Klasifikasi ini sangat penting dalam memahami sifat kimia dan reaktivitas unsur-unsur, serta dalam memprediksi bagaimana mereka akan bereaksi dalam berbagai situasi. Dengan memahami klasifikasi ini, kita dapat lebih mudah memahami interaksi antara unsur-unsur dan bagaimana mereka membentuk senyawa.
Perkembangan Tabel Periodik Unsur
Tabel Periodik Unsur (SPU) telah mengalami perkembangan signifikan sejak awalnya dikembangkan oleh Dmitri Mendeleev pada tahun 1869. Awalnya, SPU hanya berisi sekitar 63 unsur yang diketahui pada masa itu, dan disusun berdasarkan massa atom dan sifat kimia. Namun, dengan penemuan unsur-unsur baru dan pemahaman yang lebih mendalam tentang struktur atom, SPU terus diperbaiki dan disempurnakan.
Salah satu perubahan besar dalam SPU adalah pergeseran dari penggunaan nomor atom sebagai dasar penyusunan, bukan massa atom. Pada awalnya, SPU disusun berdasarkan massa atom, tetapi dengan adanya penemuan isotop dan pengukuran yang lebih akurat, para ilmuwan menyadari bahwa nomor atom lebih tepat untuk menjelaskan sifat kimia unsur. Hal ini mengarah pada pengembangan SPU modern yang digunakan saat ini.
Selain itu, pengenalan konsep orbital dan mekanika kuantum juga memberikan dasar baru untuk memahami struktur atom dan hubungan antara unsur-unsur. Dengan memahami orbit dan sub-orbit elektron, para ilmuwan dapat menjelaskan sifat-sifat periodik seperti jari-jari atom, energi ionisasi, dan elektronegativitas dengan lebih akurat.
Perkembangan SPU tidak hanya berdampak pada ilmu kimia, tetapi juga pada berbagai bidang lain seperti teknologi, farmasi, dan material. Dengan memahami SPU, kita dapat memprediksi sifat-sifat unsur dan bagaimana mereka akan bereaksi, yang sangat penting dalam pengembangan produk baru dan inovasi teknologi.
Fungsi dan Manfaat Sistem Periodik Unsur
Sistem Periodik Unsur (SPU) memiliki banyak fungsi dan manfaat dalam berbagai bidang, terutama dalam ilmu kimia. Salah satu manfaat utama dari SPU adalah kemampuannya untuk memprediksi sifat-sifat kimia dari unsur-unsur berdasarkan posisinya dalam tabel. Dengan memahami pola sifat periodik, ilmuwan dapat memperkirakan reaktivitas, kestabilan, dan kemungkinan ikatan kimia dari suatu unsur tanpa perlu melakukan eksperimen langsung.
Selain itu, SPU juga membantu dalam memahami hubungan antara struktur atom dan sifat kimia. Misalnya, dengan mengetahui jumlah elektron valensi suatu unsur, kita dapat memahami bagaimana unsur tersebut akan bereaksi dengan unsur lain. Hal ini sangat penting dalam studi kimia organik dan anorganik, serta dalam pengembangan senyawa baru.
Manfaat lain dari SPU adalah dalam industri dan teknologi. Dengan memahami sifat-sifat unsur, insinyur dan ilmuwan dapat memilih unsur yang tepat untuk aplikasi tertentu. Misalnya, logam seperti tembaga dan alumunium digunakan dalam industri listrik karena konduktivitasnya yang baik, sedangkan unsur seperti silikon digunakan dalam produksi chip komputer karena sifat semikonduktornya.
Selain itu, SPU juga menjadi alat bantu dalam pendidikan. Siswa dan mahasiswa dapat menggunakan SPU untuk mempelajari sifat-sifat kimia, memahami reaksi kimia, dan memprediksi hasil eksperimen. Dengan demikian, SPU tidak hanya berguna dalam penelitian dan industri, tetapi juga dalam pendidikan dan pengembangan ilmu pengetahuan.
Peran Sistem Periodik Unsur dalam Ilmu Kimia
Sistem Periodik Unsur (SPU) memainkan peran penting dalam ilmu kimia, baik dalam teori maupun praktik. Dengan struktur yang teratur dan logis, SPU membantu ilmuwan memahami hubungan antara sifat-sifat kimia dan struktur atom. Ini memungkinkan prediksi sifat-sifat unsur yang belum ditemukan atau belum diketahui, serta memahami reaksi kimia yang terjadi antara unsur-unsur.
Dalam teori kimia, SPU digunakan untuk menjelaskan konsep-konsep seperti konfigurasi elektron, ikatan kimia, dan sifat periodik. Misalnya, dengan memahami konfigurasi elektron, kita dapat memprediksi bagaimana suatu unsur akan bereaksi dengan unsur lain. Hal ini sangat penting dalam studi kimia organik dan anorganik, serta dalam pengembangan senyawa baru.
Dalam praktik kimia, SPU membantu dalam analisis dan sintesis senyawa. Dengan mengetahui sifat-sifat kimia dari suatu unsur, ilmuwan dapat memilih unsur yang tepat untuk reaksi tertentu. Misalnya, logam seperti natrium dan kalium digunakan dalam reaksi redoks karena sifat reduktor mereka yang kuat, sedangkan unsur seperti klorin digunakan dalam reaksi oksidasi karena sifat oksidatornya yang kuat.
Selain itu, SPU juga digunakan dalam industri dan teknologi. Dengan memahami sifat-sifat unsur, insinyur dan ilmuwan dapat memilih unsur yang sesuai untuk aplikasi tertentu. Misalnya, logam seperti emas dan perak digunakan dalam industri elektronik karena konduktivitasnya yang baik, sedangkan unsur seperti silikon digunakan dalam produksi chip komputer karena sifat semikonduktornya.
Dengan demikian, SPU tidak hanya menjadi alat bantu dalam ilmu kimia, tetapi juga menjadi dasar bagi berbagai bidang lain seperti teknologi, farmasi, dan material. Dengan memahami SPU, kita dapat lebih mudah memahami sifat-sifat kimia dan bagaimana unsur-unsur berinteraksi satu sama lain.


0Komentar