Kimia adalah ilmu yang mempelajari sifat, komposisi, struktur, dan perubahan materi. Dalam studi kimia, salah satu aspek penting yang sering dipelajari adalah stoikiometri. Stoikiometri merupakan bagian dari ilmu kimia yang mempelajari tentang kuantitas atau jumlah zat dalam suatu reaksi kimia. Kata "stoikiometri" berasal dari bahasa Yunani, yaitu stoicheion yang berarti elemen dan metron yang berarti mengukur. Jadi, secara sederhana, stoikiometri berkaitan dengan pengukuran elemen dalam reaksi kimia.
Stoikiometri digunakan untuk menentukan hubungan antara jumlah zat pereaksi dan produk dalam suatu reaksi. Dengan menggunakan stoikiometri, kita dapat menghitung jumlah mol, massa, volume, atau partikel dari suatu zat berdasarkan persamaan reaksi yang seimbang. Ini sangat penting dalam praktik laboratorium maupun dalam industri, karena memastikan bahwa reaksi berlangsung secara efisien dan tanpa kelebihan atau kekurangan bahan baku.
Dalam artikel ini, kita akan membahas lebih lanjut tentang apa itu stoikiometri, bagaimana cara menentukan rumus molekul dan rumus empiris, serta konsep-konsep dasar stoikiometri seperti hukum-hukum dasar kimia, konsep mol, molaritas, dan jenis-jenis stoikiometri. Selain itu, kita juga akan melihat contoh soal stoikiometri untuk memperkuat pemahaman tentang topik ini.
Apa Itu Stoikiometri?
Stoikiometri adalah ilmu kimia yang mempelajari tentang kuantitas zat dalam suatu reaksi kimia. Dalam istilah sederhana, stoikiometri membantu kita memahami bagaimana zat-zat berinteraksi dalam suatu reaksi dan bagaimana jumlahnya saling terkait. Misalnya, jika kita ingin mengetahui seberapa banyak oksigen diperlukan untuk bereaksi dengan hidrogen membentuk air, stoikiometri akan memberikan jawabannya.
Stoikiometri berasal dari kata Yunani stoicheion (elemen) dan metron (mengukur), yang menggambarkan konsep utamanya: mengukur kuantitas elemen dalam reaksi kimia. Ilmu ini sangat penting dalam bidang kimia, terutama dalam analisis senyawa, penyetaraan reaksi, dan perhitungan kuantitas zat.
Penggunaan stoikiometri tidak hanya terbatas pada laboratorium, tetapi juga dalam industri, misalnya dalam produksi obat, bahan bakar, dan bahan kimia lainnya. Dengan stoikiometri, kita bisa memastikan bahwa reaksi berlangsung sesuai dengan proporsi yang ideal, sehingga tidak ada bahan baku yang terbuang sia-sia.
Konsep Dasar Stoikiometri
Untuk memahami stoikiometri, kita perlu mengenal beberapa konsep dasar yang menjadi fondasi dalam studi ini. Berikut adalah beberapa konsep penting:
- Rumus Molekul dan Rumus Empiris
- Rumus Molekul: Menunjukkan jumlah atom setiap unsur dalam suatu senyawa. Contohnya, rumus molekul air adalah H₂O, yang berarti terdiri dari dua atom hidrogen dan satu atom oksigen.
-
Rumus Empiris: Merupakan perbandingan terkecil dari jumlah atom dalam suatu senyawa. Contohnya, rumus empiris glukosa (C₆H₁₂O₆) adalah CH₂O.
-
Massa Atom Relatif (Ar)
Massa atom relatif adalah perbandingan massa satu atom dengan 1/12 massa isotop karbon-12 (C-12). Ar digunakan untuk menentukan massa molekul relatif suatu senyawa. -
Massa Molekul Relatif (Mr)
Massa molekul relatif adalah jumlah massa atom relatif dari semua atom dalam suatu molekul. Misalnya, Mr air (H₂O) adalah 18, karena Ar H = 1 dan Ar O = 16. -
Konsep Mol
Satu mol suatu zat mengandung 6,02 x 10²³ partikel (Avogadro's number). Mol digunakan untuk menghubungkan jumlah partikel dengan massa atau volume suatu zat. -
Molaritas (M)
Molaritas adalah jumlah mol zat terlarut dalam satu liter larutan. Rumus molaritas adalah M = n/V, di mana n adalah jumlah mol dan V adalah volume larutan dalam liter. -
Hukum-Hukum Dasar Kimia
Beberapa hukum dasar kimia yang terkait dengan stoikiometri antara lain: - Hukum Kekekalan Massa: Massa total sebelum dan sesudah reaksi sama.
- Hukum Perbandingan Tetap: Perbandingan massa unsur dalam suatu senyawa selalu tetap.
- Hukum Perbandingan Berganda: Jika dua unsur membentuk lebih dari satu senyawa, perbandingan massa salah satu unsur adalah bilangan bulat sederhana.
-
Hukum Perbandingan Volume: Volume gas yang bereaksi dan hasil reaksi memiliki perbandingan yang sederhana jika diukur pada suhu dan tekanan yang sama.
-
Jenis-Jenis Stoikiometri
- Stoikiometri Reaksi: Mempelajari hubungan antara jumlah zat dalam reaksi kimia.
- Stoikiometri Komposisi: Mempelajari hubungan antar unsur dalam suatu senyawa.
- Stoikiometri Gas: Mempelajari reaksi kimia yang melibatkan gas.
Dengan memahami konsep-konsep dasar ini, kita dapat lebih mudah memahami dan menerapkan stoikiometri dalam berbagai situasi, baik dalam studi kimia maupun dalam kehidupan sehari-hari.
Cara Menentukan Rumus Molekul dan Rumus Empiris
Dalam stoikiometri, menentukan rumus molekul dan rumus empiris adalah langkah penting untuk memahami komposisi suatu senyawa. Berikut adalah cara-cara yang digunakan:
1. Menentukan Rumus Empiris
Rumus empiris adalah perbandingan terkecil dari jumlah atom dalam suatu senyawa. Untuk menentukan rumus empiris, kita dapat menggunakan dua metode:
-
Melalui Rumus Molekul:
Jika rumus molekul diketahui, kita dapat menyederhanakan jumlah atom penyusunnya agar diperoleh bilangan bulat paling kecil.
Contoh:
Rumus molekul C₆H₁₂O₆ dapat disederhanakan menjadi CH₂O, sehingga rumus empirisnya adalah CH₂O. -
Melalui Perbandingan Mol:
Jika massa unsur-unsur dalam senyawa diketahui, kita dapat menghitung jumlah mol masing-masing unsur, lalu mencari perbandingan terkecilnya.
Contoh:
Jika suatu senyawa mengandung 40% unsur X (Ar = 32) dan 60% unsur Y (Ar = 16), maka: - Mol X = 40 / 32 = 1,25
- Mol Y = 60 / 16 = 3,75
- Perbandingan mol X : Y = 1,25 : 3,75 = 1 : 3
Sehingga rumus empirisnya adalah XY₃.
2. Menentukan Rumus Molekul
Rumus molekul adalah kelipatan dari rumus empiris. Untuk menentukan rumus molekul, kita perlu mengetahui massa molekul relatif (Mr) dari senyawa tersebut. Rumus yang digunakan adalah:
$$ \text{Mr}{\text{molekul}} = \text{Mr} \times n $$}
Di mana $n$ adalah kelipatan dari rumus empiris terhadap rumus molekul.
Contoh:
Jika Mr suatu senyawa adalah 80 dan rumus empirisnya adalah XY₃ (Mr = 32 + 3×16 = 80), maka rumus molekulnya adalah XY₃.
Dengan mengetahui cara menentukan rumus molekul dan rumus empiris, kita dapat lebih mudah memahami struktur dan komposisi senyawa dalam stoikiometri.
Konsep Mol dan Hubungannya dengan Stoikiometri
Konsep mol adalah salah satu fondasi utama dalam stoikiometri. Mol digunakan untuk menghubungkan jumlah partikel dengan massa atau volume suatu zat. Berikut adalah penjelasan lebih rinci tentang konsep mol dan hubungannya dengan stoikiometri:
1. Definisi Mol
Satu mol suatu zat mengandung 6,02 × 10²³ partikel, yang dikenal sebagai tetapan Avogadro. Partikel ini bisa berupa atom, molekul, ion, atau partikel lainnya. Dengan demikian, mol adalah satuan yang digunakan untuk mengukur jumlah zat dalam stoikiometri.
2. Hubungan Mol dengan Massa
Massa suatu zat dapat dihitung dari jumlah molnya menggunakan massa molar, yaitu massa satu mol zat. Massa molar dihitung berdasarkan massa atom relatif (Ar) dari setiap atom dalam molekul.
Contoh:
Massa molar air (H₂O) adalah:
- H = 1 g/mol × 2 = 2 g/mol
- O = 16 g/mol
Total = 2 + 16 = 18 g/mol
Jadi, 1 mol air memiliki massa 18 gram.
3. Hubungan Mol dengan Volume Gas
Pada kondisi standar (STP), 1 mol gas ideal memiliki volume 22,4 L. Karena itu, kita dapat menghitung volume gas berdasarkan jumlah molnya.
Contoh:
Jika kita memiliki 0,5 mol gas oksigen (O₂), maka volumenya adalah:
0,5 mol × 22,4 L/mol = 11,2 L
4. Hubungan Mol dengan Jumlah Partikel
Karena satu mol mengandung 6,02 × 10²³ partikel, kita dapat menghitung jumlah partikel dari jumlah mol yang diketahui.
Contoh:
Jika kita memiliki 2 mol air (H₂O), maka jumlah molekulnya adalah:
2 mol × 6,02 × 10²³ = 1,204 × 10²⁴ molekul
Dengan memahami konsep mol dan hubungannya dengan stoikiometri, kita dapat melakukan berbagai perhitungan dalam reaksi kimia, seperti menentukan jumlah zat yang dibutuhkan atau dihasilkan.
Jenis-Jenis Stoikiometri
Dalam ilmu kimia, stoikiometri dibagi menjadi tiga jenis utama, yaitu:
1. Stoikiometri Reaksi
Stoikiometri reaksi mempelajari hubungan antara jumlah zat dalam suatu reaksi kimia. Dalam stoikiometri reaksi, kita biasanya menyetarakan persamaan reaksi dan menghitung jumlah zat pereaksi dan produk berdasarkan koefisien stoikiometri.
Contoh:
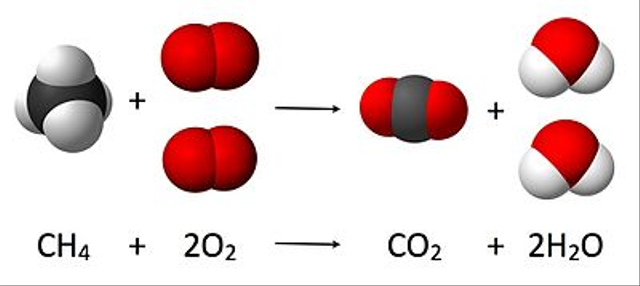
Reaksi pembakaran metana (CH₄):
CH₄ + 2O₂ → CO₂ + 2H₂O
Dari persamaan ini, kita tahu bahwa 1 mol CH₄ bereaksi dengan 2 mol O₂ untuk menghasilkan 1 mol CO₂ dan 2 mol H₂O.
2. Stoikiometri Komposisi
Stoikiometri komposisi mempelajari hubungan antar unsur dalam suatu senyawa. Dengan stoikiometri komposisi, kita dapat menentukan rumus molekul dan rumus empiris suatu senyawa berdasarkan perbandingan massa atau jumlah mol unsur-unsurnya.
Contoh:
Jika suatu senyawa mengandung 40% karbon (Ar = 12) dan 60% oksigen (Ar = 16), maka perbandingan molnya adalah:
- Karbon = 40 / 12 ≈ 3,33
- Oksigen = 60 / 16 = 3,75
Perbandingan terkecilnya adalah 1 : 1,25, sehingga rumus empirisnya adalah CO₁,25, yang kemudian disederhanakan menjadi C₂O₅.
3. Stoikiometri Gas
Stoikiometri gas mempelajari reaksi kimia yang melibatkan gas. Dalam stoikiometri gas, kita menggunakan hukum-hukum gas seperti Hukum Charles, Hukum Boyle, dan Hukum Gay-Lussac untuk menghitung volume, tekanan, atau suhu gas.
Contoh:
Jika 2 mol gas hidrogen (H₂) bereaksi dengan 1 mol gas oksigen (O₂) membentuk 2 mol uap air (H₂O), maka volume gas yang bereaksi dapat dihitung berdasarkan hukum perbandingan volume.
Dengan memahami ketiga jenis stoikiometri ini, kita dapat lebih mudah menerapkannya dalam berbagai situasi, baik dalam studi kimia maupun dalam kehidupan sehari-hari.
Contoh Soal Stoikiometri
Untuk memperdalam pemahaman tentang stoikiometri, berikut adalah beberapa contoh soal beserta penyelesaiannya:
Contoh Soal 1: Menentukan Rumus Molekul
Suatu senyawa memiliki Mr = 80 dan mengandung 40% unsur X (Ar = 32) dan sisanya adalah Y (Ar = 16). Tentukan rumus molekul senyawa tersebut!
Penyelesaian:
- Massa X = 40% dari 80 = 32 g
- Massa Y = 60% dari 80 = 48 g
- Mol X = 32 / 32 = 1 mol
- Mol Y = 48 / 16 = 3 mol
- Perbandingan mol X : Y = 1 : 3
Sehingga rumus empirisnya adalah XY₃.
Karena Mr XY₃ = 32 + 3×16 = 80, maka rumus molekulnya adalah XY₃.
Contoh Soal 2: Menghitung Volume Gas
Jika 12,8 gram SO₂ direaksikan dengan O₂ berdasarkan reaksi:
2SO₂ + O₂ → 2SO₃
Tentukan volume O₂ yang diperlukan pada STP!
Penyelesaian:
- Mr SO₂ = 32 + 2×16 = 64 g/mol
- Mol SO₂ = 12,8 / 64 = 0,2 mol
- Dari reaksi, perbandingan mol SO₂ : O₂ = 2 : 1
- Mol O₂ = 0,2 / 2 = 0,1 mol
- Volume O₂ = 0,1 mol × 22,4 L/mol = 2,24 L
Contoh Soal 3: Pereaksi Pembatas
Sebanyak 22 gram C₃H₈ direaksikan dengan 48 gram O₂ berdasarkan reaksi:
C₃H₈ + 5O₂ → 3CO₂ + 4H₂O
Tentukan pereaksi pembatas dan massa zat yang tersisa!
Penyelesaian:
- Mr C₃H₈ = 44 g/mol → Mol = 22 / 44 = 0,5 mol
- Mr O₂ = 32 g/mol → Mol = 48 / 32 = 1,5 mol
- Dari reaksi, perbandingan mol C₃H₈ : O₂ = 1 : 5
- Jumlah O₂ yang dibutuhkan = 0,5 × 5 = 2,5 mol
- Karena hanya ada 1,5 mol O₂, maka O₂ adalah pereaksi pembatas.
- Mol C₃H₈ yang bereaksi = 1,5 / 5 = 0,3 mol
- Mol C₃H₈ yang tersisa = 0,5 - 0,3 = 0,2 mol
- Massa C₃H₈ tersisa = 0,2 × 44 = 8,8 gram
Dengan menyelesaikan contoh soal-soal ini, kita dapat lebih memahami aplikasi stoikiometri dalam berbagai situasi.


0Komentar