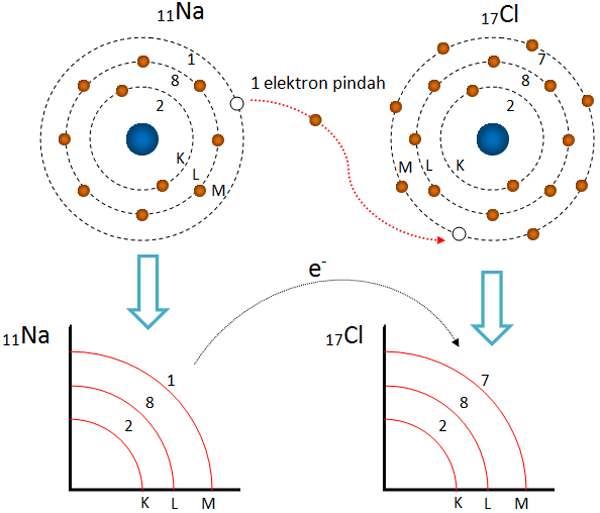
Contoh Ikatan Ion dan Cara Terbentuknya dalam Kimia
Dalam dunia kimia, interaksi antara unsur-unsur membentuk senyawa yang sangat penting dalam kehidupan sehari-hari. Salah satu contoh paling umum adalah garam dapur (NaCl), yang terbentuk melalui ikatan ion. Ikatan ion merupakan salah satu jenis ikatan kimia yang terjadi antara unsur logam dan nonlogam, dengan proses serah terima elektron. Proses ini tidak hanya memengaruhi sifat senyawa yang dihasilkan, tetapi juga berkontribusi pada banyak fenomena alami dan teknologi modern.
Ikatan ion memiliki peran krusial dalam membentuk struktur padat dari senyawa-senyawa seperti garam, oksida logam, dan hidroksida. Sifat-sifat unik dari senyawa ion seperti titik leleh tinggi, kemampuan menghantarkan listrik saat larut, serta kelarutan dalam air menjadikannya penting dalam bidang industri, pertanian, dan bahkan biologi. Untuk memahami lebih dalam tentang ikatan ion, kita perlu mengeksplorasi pengertian, cara terbentuknya, serta contoh-contoh nyata dari ikatan ini.
Pengertian ikatan ion bermula dari konsep dasar kimia, yaitu stabilitas atom. Atom-atom cenderung mencapai kestabilan dengan memiliki konfigurasi elektron yang mirip dengan gas mulia, yaitu 2 atau 8 elektron di kulit terluarnya. Unsur logam biasanya melepaskan elektron untuk mencapai konfigurasi tersebut, sedangkan unsur nonlogam menerima elektron. Proses ini menghasilkan ion positif (kation) dan ion negatif (anion), yang saling tarik-menarik karena perbedaan muatan. Gaya elektrostatik inilah yang menjadi dasar dari ikatan ion.
Selain itu, ikatan ion memiliki karakteristik khas seperti kekuatan ikatan yang kuat, sehingga senyawa ion umumnya keras dan rapuh. Meskipun demikian, senyawa ini mudah larut dalam air karena interaksi antara ion dan molekul air. Pemahaman tentang ikatan ion tidak hanya berguna dalam studi ilmu kimia, tetapi juga memberikan wawasan tentang bagaimana materi berinteraksi di sekitar kita.
Pengertian Ikatan Ion
Ikatan ion adalah ikatan kimia yang terbentuk antara dua atom yang memiliki perbedaan besar dalam keelektronegatifan. Biasanya, ikatan ini terjadi antara unsur logam dan nonlogam. Unsur logam cenderung melepaskan elektron, sedangkan unsur nonlogam cenderung menerima elektron. Proses ini menghasilkan ion positif (kation) dan ion negatif (anion). Kedua ion ini saling tarik-menarik karena perbedaan muatan, membentuk struktur kristal yang stabil.
Keterlibatan elektron valensi dalam ikatan ion sangat penting. Elektron valensi adalah elektron yang berada di kulit terluar atom dan bertanggung jawab atas reaktivitas kimia. Dalam ikatan ion, atom logam melepaskan elektron valensinya, sedangkan atom nonlogam menerima elektron tersebut. Misalnya, natrium (Na) melepaskan satu elektron valensi untuk menjadi Na⁺, sedangkan klorin (Cl) menerima satu elektron untuk menjadi Cl⁻. Interaksi antara Na⁺ dan Cl⁻ membentuk senyawa NaCl, yang dikenal sebagai garam dapur.
Proses pembentukan ikatan ion bisa dipahami melalui langkah-langkah berikut:
- Sublimasi: Atom logam berubah dari bentuk padat menjadi uap.
- Ionisasi: Atom logam melepaskan elektron, membentuk ion positif.
- Disosiasi: Molekul nonlogam terurai menjadi atom-atom individu.
- Elektron Affinity: Atom nonlogam menerima elektron, membentuk ion negatif.
- Formasi Kristal: Ion positif dan negatif saling tarik-menarik, membentuk struktur kristal yang stabil.
Dengan memahami proses ini, kita dapat melihat bagaimana ikatan ion terbentuk secara alami dan bagaimana senyawa-senyawa yang dihasilkan memiliki sifat-sifat khas.
Ciri-Ciri Ikatan Ion
Ikatan ion memiliki beberapa ciri khas yang membedakannya dari jenis ikatan lain, seperti ikatan kovalen. Berikut adalah beberapa ciri utama dari ikatan ion:
-
Terbentuk oleh Serah Terima Elektron: Ikatan ion terjadi ketika satu atom melepaskan elektron dan atom lain menerima elektron. Ini berbeda dari ikatan kovalen, di mana elektron dibagikan antara dua atom.
-
Keterlibatan Unsur Logam dan Nonlogam: Ikatan ion biasanya terjadi antara logam dan nonlogam. Logam cenderung melepaskan elektron, sedangkan nonlogam cenderung menerima elektron.
-
Struktur Kristal: Senyawa ion umumnya memiliki struktur kristal yang teratur. Struktur ini disebabkan oleh gaya elektrostatik antara ion positif dan negatif.
-
Titik Leleh dan Titik Didih Tinggi: Karena ikatan ion sangat kuat, senyawa ion memiliki titik leleh dan titik didih yang tinggi. Contohnya, garam dapur (NaCl) memiliki titik leleh sekitar 801°C.
-
Menghantarkan Listrik dalam Larutan atau Lelehan: Senyawa ion dapat menghantarkan arus listrik jika dilelehkan atau dilarutkan dalam air. Hal ini karena ion-ion bebas bergerak dalam larutan atau lelehan.
-
Kelarutan dalam Air: Banyak senyawa ion mudah larut dalam air karena interaksi antara ion dan molekul air. Namun, senyawa ion umumnya sulit larut dalam pelarut organik.
-
Sifat Keras dan Rapuh: Senyawa ion biasanya keras dan rapuh karena struktur kristal yang kuat. Jika diberi tekanan, struktur ini bisa pecah.
Dengan memahami ciri-ciri ini, kita dapat mengidentifikasi senyawa-senyawa yang memiliki ikatan ion dan memahami sifat-sifatnya.
Proses Terbentuknya Ikatan Ion
Proses terbentuknya ikatan ion melibatkan serah terima elektron antara dua atom. Langkah-langkahnya dapat dijelaskan sebagai berikut:
-
Atom Logam Melepaskan Elektron: Atom logam, seperti natrium (Na), memiliki elektron valensi yang relatif mudah dilepaskan. Misalnya, natrium melepaskan satu elektron untuk mencapai konfigurasi elektron yang stabil.
-
Reaksi: Na → Na⁺ + e⁻
-
Atom Nonlogam Menerima Elektron: Atom nonlogam, seperti klorin (Cl), memiliki kecenderungan untuk menerima elektron agar mencapai konfigurasi stabil. Misalnya, klorin menerima satu elektron.
-
Reaksi: Cl + e⁻ → Cl⁻
-
Interaksi Antara Ion Positif dan Negatif: Setelah terbentuk ion positif dan negatif, mereka saling tarik-menarik karena perbedaan muatan. Gaya elektrostatik ini menghasilkan ikatan ion yang stabil.
-
Reaksi: Na⁺ + Cl⁻ → NaCl
-
Bentuk Struktur Kristal: Ion-ion positif dan negatif saling mengelilingi, membentuk struktur kristal yang sangat teratur. Struktur ini menjaga kestabilan senyawa ion.
Contoh lain dari proses ini adalah pembentukan kalium klorida (KCl). Kalium (K) melepaskan satu elektron untuk menjadi K⁺, sedangkan klorin (Cl) menerima satu elektron untuk menjadi Cl⁻. Interaksi antara K⁺ dan Cl⁻ membentuk senyawa KCl.
Proses ini juga terjadi dalam pembentukan aluminium oksida (Al₂O₃). Aluminium (Al) melepaskan tiga elektron untuk menjadi Al³⁺, sedangkan oksigen (O) menerima dua elektron untuk menjadi O²⁻. Interaksi antara ion-ion ini membentuk senyawa Al₂O₃.
Contoh Ikatan Ion
Beberapa contoh ikatan ion yang umum dapat ditemukan dalam kehidupan sehari-hari dan dalam laboratorium. Berikut adalah beberapa contoh ikatan ion beserta penjelasannya:
-
Natrium Klorida (NaCl)
Natrium klorida, atau garam dapur, adalah contoh ikatan ion yang paling dikenal. Natrium (Na) melepaskan satu elektron, sedangkan klorin (Cl) menerima satu elektron. Hasilnya, Na⁺ dan Cl⁻ saling tarik-menarik, membentuk senyawa NaCl. -
Kalium Klorida (KCl)
Kalium klorida terbentuk dari interaksi antara kalium (K) dan klorin (Cl). Kalium melepaskan satu elektron, sedangkan klorin menerima satu elektron. Hasilnya, K⁺ dan Cl⁻ membentuk senyawa KCl. -
Aluminium Oksida (Al₂O₃)
Aluminium oksida terbentuk dari interaksi antara aluminium (Al) dan oksigen (O). Aluminium melepaskan tiga elektron, sedangkan oksigen menerima dua elektron. Hasilnya, Al³⁺ dan O²⁻ membentuk senyawa Al₂O₃. -
Kalsium Oksida (CaO)
Kalsium oksida terbentuk dari interaksi antara kalsium (Ca) dan oksigen (O). Kalsium melepaskan dua elektron, sedangkan oksigen menerima dua elektron. Hasilnya, Ca²⁺ dan O²⁻ membentuk senyawa CaO. -
Magnesium Klorida (MgCl₂)
Magnesium klorida terbentuk dari interaksi antara magnesium (Mg) dan klorin (Cl). Magnesium melepaskan dua elektron, sedangkan dua atom klorin masing-masing menerima satu elektron. Hasilnya, Mg²⁺ dan dua Cl⁻ membentuk senyawa MgCl₂.
Setiap contoh ini menunjukkan bagaimana ikatan ion terbentuk melalui serah terima elektron antara logam dan nonlogam. Proses ini menghasilkan senyawa yang stabil dan memiliki sifat-sifat khas.
Perbedaan Ikatan Ion dan Ikatan Kovalen
Meskipun ikatan ion dan ikatan kovalen sama-sama merupakan jenis ikatan kimia, keduanya memiliki perbedaan signifikan dalam cara terbentuknya dan sifat-sifatnya. Berikut adalah beberapa perbedaan utama antara keduanya:
- Jenis Unsur yang Terlibat
- Ikatan Ion: Terjadi antara unsur logam dan nonlogam.
-
Ikatan Kovalen: Terjadi antara dua atom nonlogam.
-
Mekanisme Pembentukan
- Ikatan Ion: Melibatkan serah terima elektron antara atom logam dan nonlogam.
-
Ikatan Kovalen: Melibatkan pembagian pasangan elektron antara dua atom nonlogam.
-
Muatan Ion
- Ikatan Ion: Menghasilkan ion positif (kation) dan ion negatif (anion).
-
Ikatan Kovalen: Tidak menghasilkan ion, tetapi membentuk molekul netral.
-
Sifat Fisika
- Ikatan Ion: Memiliki titik leleh dan titik didih tinggi, mudah larut dalam air, dan dapat menghantarkan listrik dalam larutan.
-
Ikatan Kovalen: Umumnya memiliki titik leleh dan titik didih rendah, kurang larut dalam air, dan tidak dapat menghantarkan listrik.
-
Struktur Molekul
- Ikatan Ion: Membentuk struktur kristal yang teratur.
-
Ikatan Kovalen: Membentuk molekul individual yang tidak memiliki struktur kristal.
-
Contoh Senyawa
- Ikatan Ion: NaCl, KCl, Al₂O₃, CaO.
- Ikatan Kovalen: H₂O, CO₂, CH₄, O₂.
Perbedaan ini menunjukkan bahwa setiap jenis ikatan memiliki peran dan sifat yang berbeda dalam dunia kimia. Memahami perbedaan ini membantu kita mengidentifikasi senyawa dan memprediksi sifat-sifatnya.
Kesimpulan
Ikatan ion adalah salah satu jenis ikatan kimia yang sangat penting dalam memahami struktur dan sifat senyawa. Proses terbentuknya ikatan ion melibatkan serah terima elektron antara atom logam dan nonlogam, menghasilkan ion positif dan negatif yang saling tarik-menarik. Contoh ikatan ion yang umum termasuk natrium klorida (NaCl), kalium klorida (KCl), dan aluminium oksida (Al₂O₃).
Dengan memahami konsep dasar ikatan ion, kita dapat lebih mudah memahami sifat-sifat senyawa yang dihasilkan dan aplikasinya dalam kehidupan sehari-hari. Selain itu, membandingkan ikatan ion dengan ikatan kovalen memberikan wawasan lebih dalam tentang perbedaan mekanisme dan sifat fisika antara kedua jenis ikatan ini.
Dengan demikian, ikatan ion tidak hanya menjadi dasar dari banyak senyawa yang kita temui sehari-hari, tetapi juga menjadi fondasi penting dalam studi kimia dan aplikasinya di berbagai bidang.


0Komentar